Wreszcie pojawiło się rozporządzenie w sprawie reklamy wyrobów medycznych! Co w praktyce zmienia ten dokument? Jakie są wnioski dla właścicieli gabinetów beauty? Co trzeba umieszczać w reklamach zabiegów z wykorzystaniem wyrobów medycznych?
Rozporządzenie w sprawie reklamy wyrobów medycznych – w skrócie: o co chodzi?
Mniej więcej rok temu weszła w życie nowa ustawa o wyrobach medycznych. Część ustawy dotycząca reklamy wyrobów medycznych zaczęła obowiązywać nieco później, bo od 1 stycznia 2023 roku. Temat szczegółowo omawiałam już w wielu artykułach (klik), a także w e-booku ZAKAZ REKLAMY – fakty, mity, pytania i odpowiedzi – Co zmienia ustawa o wyrobach medycznych? Co można, a czego nie? (klik).
Dziś przytoczę tylko jeden zapis ustawy (klik), który zapowiadał wydanie aktualnego rozporządzenia:
4. Minister właściwy do spraw zdrowia określi, w drodze rozporządzenia:
1) niezbędne dane, jakie ma zawierać reklama, inne niż określone w ust. 3,
2) sposób prezentowania reklamy
– uwzględniając konieczność obiektywnej prezentacji wyrobu, bezpieczeństwo jego stosowania, stan wiedzy użytkowników wyrobów oraz konieczność zapewnienia niezakłóconego korzystania z usług zdrowotnych i usług farmaceutycznych.
Oprócz szeregu wymagań dotyczących reklam, które zostały zapisane w samej ustawie, otrzymaliśmy zapowiedź doprecyzowania wymogów w formie rozporządzenia.
Rozporządzenie miało pojawić się pod koniec ubiegłego roku. Opublikowano je jednak dopiero pod koniec kwietnia z datą wejścia w życie 13 maja. Z pełną treścią rozporządzenia możesz zapoznać się tutaj.
Co zawiera rozporządzenie w sprawie reklamy wyrobów medycznych?
O pomoc w interpretacji zapisów rozporządzenia poprosiłam radcę prawnego Marka Koennera, współautora wspomnianego już e-booka ZAKAZ REKLAMY – fakty, mity, pytania i odpowiedzi – Co zmienia ustawa o wyrobach medycznych? Co można, a czego nie? (klik).
Przeanalizujemy wspólnie kolejne fragmenty dokumentu, szukając odpowiedzi na pytanie:
Co to w praktyce oznacza dla właściciela salonu beauty, który chce reklamować zabiegi z wykorzystaniem wyrobów medycznych?
Fragment rozporządzenia:
§ 2. Dane dotyczące wyrobu przekazuje się w brzmieniu zgodnym z instrukcją używania wyrobu lub etykietą reklamowanego wyrobu i przedstawia się je w formie:
1) audiowizualnej i wizualnej w sposób widoczny i czytelny;
2) dźwiękowej w sposób wyraźny.
ANNA WYDRA-NAZIMEK: Brzmi to odrobinę enigmatycznie… Jak to rozumieć?
MAREK KOENNER: Oznacza to tyle, że wszystkie dane i informacje dotyczące zabiegu, które będziemy przekazywać w reklamie, muszą być zgodne z tymi zawartymi w instrukcji używania lub z etykietą wyrobu medycznego, za pomocą którego będzie wykonywany ten zabieg.
Pamiętajmy, że zgodnie z art. 60 ust. o wyrobach medycznych każda reklama musi zawierać co najmniej nazwę lub nazwę handlową oraz przewidziane zastosowanie wyrobu.
Czyli tak jak to tłumaczyliśmy w e-booku – jeżeli w instrukcji nie będzie napisane, że urządzenie ma zastosowanie do redukcji „kurzych łapek”, to nie możemy w reklamie wskazywać lub sugerować, że takie zastosowanie ma. Ponadto w reklamie będziemy musieli podać nazwę wyrobu medycznego wskazaną na etykiecie, a nie nazwę zwyczajowo/branżowo przyjętą dla tego typu wyrobu.
Wszystkie dane, które będziemy podawać o wyrobie, muszą być zgodne z etykietą lub instrukcją wyrobu.
Dane o wyrobie powinny być przekazywane:
1) w sposób widoczny i czytelny w przypadku reklamy w postaci rolki lub filmiku w social mediach, a także w postaci zdjęć i plakatów (czyli z wykorzystaniem obrazu, dźwięku i ruchu, lub wyłącznie obrazu),
2) w sposób wyraźny w przypadku reklamy w postaci wyłącznie dźwiękowej np. reklamy w radiu.
Nie możemy więc np. używać czcionek, kolorów, obrazów, które wpływają na trudność z odczytaniem informacji o danym wyrobie.
Fragment rozporządzenia:
Reklama wyrobu medycznego oraz wyrobu medycznego do diagnostyki in vitro kierowana do publicznej wiadomości zawiera:
1) określenie podmiotu prowadzącego reklamę;
2) nazwę producenta i upoważnionego przedstawiciela, jeżeli został wyznaczony;
3) ostrzeżenie o następującej treści: „To jest wyrób medyczny. Używaj go zgodnie z instrukcją używania lub etykietą.”
Te zalecenia wydają się być jasne, ale nie do końca potrafię sobie wyobrazić, jak miałoby to wyglądać w praktyce. Na przykład wrzucam post reklamujący zabieg wykonywany na urządzeniu będącym wyrobem medycznym.
Co mam dopisać oprócz treści reklamowej? Czy mam dopisywać nazwę firmy, skoro publikuję post z profilu firmowego? Czy muszę podawać nazwę producenta?
Te zalecenia brzmią jak zalecenia do reklam telewizyjnych jakichś produktów dostępnych w aptece. Jak to się ma do zabiegów? Czy w reklamie np. depilacji laserowej wykonywanej na urządzeniu, które jest wyrobem medycznym, muszę dopisać „To jest wyrób medyczny. Używaj go zgodnie z instrukcją używania lub etykietą”? Z jaką instrukcją, z jaką etykietą? Przecież klient osobiście nie używa tego urządzenia. To my je używamy.
Niestety, choć rzeczywiście wymogi te pasują bardziej do typowej reklamy „sprzedażowej” prowadzonej przez producentów wyrobów, to zgodnie z przepisami ustawy o wyrobach medycznych i rozporządzeniem w reklamie zabiegów będziemy musieli obowiązkowo umieścić oprócz samej treści reklamowej:
1) określenie podmiotu prowadzącego reklamę – i to nawet jeżeli reklamę będziemy publikować z profilu firmowego,
2) nazwę lub nazwę handlową wyrobu oraz z nazwę jego producenta i upoważnionego przedstawiciela, jeżeli został wyznaczony
3) przewidziane zastosowanie wyrobu,
4) ostrzeżenie o następującej treści: „To jest wyrób medyczny. Używaj go zgodnie z instrukcją używania lub etykietą.”
To prawda to nie my będziemy używać tego urządzenia, ale pamiętajmy, że reklamować możemy wyłącznie wyroby przeznaczone dla laików, czyli takie, które może też teoretycznie nabyć i używać klient. Reklama działalności, do której wykorzystuje się wyrób medyczny traktowana jest jak reklama samego wyrobu – pośrednio bowiem też reklamuje ten wyrób.
Fragment rozporządzenia:
Reklama produktu niemającego przewidzianego zastosowania medycznego, o którym mowa w art. 1 ust. 2 rozporządzenia Parlamentu Europejskiego i Rady (UE) 2017/745 z dnia 5 kwietnia 2017 r. w sprawie wyrobów medycznych, zmiany dyrektywy 2001/83/WE, rozporządzenia (WE) nr 178/2002 i rozporządzenia (WE) nr 1223/2009 oraz uchylenia dyrektyw Rady 90/385/EWG i 93/42/EWG, wymienionego w załączniku XVI do tego rozporządzenia, oraz wyposażenia wyrobu medycznego kierowana do publicznej wiadomości zawiera:
1) określenie podmiotu prowadzącego reklamę;
2) nazwę producenta i upoważnionego przedstawiciela, jeżeli został wyznaczony;
3) ostrzeżenie o następującej treści: „Dla bezpieczeństwa używaj zgodnie z instrukcją używania lub etykietą.”.
Tutaj mamy bardzo podobny zapis, ale dotyczy on innego rodzaju produktów. Jakich konkretnie? Na czym polega różnica z poprzednim punktem?
Poprzedni punkt to jest ustęp 1 § 2. Rozporządzenia dotyczył reklamy wyrobów medycznych przeznaczonych dla laików, ten zaś dotyczy reklamy produktów niemających przewidzianego zastosowania medycznego oraz reklamy wyposażenia medycznego.
Do produktów niemających przewidzianego zastosowania medycznego zalicza się:
1. Soczewki kontaktowe lub inne przedmioty przeznaczone do wprowadzania do oka lub na oko.
2. Produkty przewidziane do całkowitego lub częściowego wprowadzenia za pomocą inwazyjnych środków chirurgicznych do ciała ludzkiego w celu zmiany anatomii lub unieruchamiania części ciała, z wyjątkiem produktów do tatuażu i piercingu.
3. Substancje, mieszaniny substancji lub artykuły przeznaczone do stosowania przy wypełnianiu skóry twarzy lub innej błony skórnej lub śluzowej w drodze wstrzykiwania podskórnego, podśluzówkowego lub śródskórnego lub innego wprowadzania, z wyjątkiem przeznaczonych do tatuażu.
4. Sprzęt przeznaczony do stosowania w celu zredukowania, usunięcia lub zniszczenia tkanki tłuszczowej, taki jak sprzęt do liposukcji, lipolizy lub lipoplastyki.
5. Sprzęt emitujący promieniowanie elektromagnetyczne o wysokim natężeniu (np. podczerwień, światło widzialne i nadfioletowe) przewidziany do stosowania na ciele ludzkim, w tym źródła spójne i niespójne, monochromatyczne i o szerokim spektrum, takie jak lasery i sprzęt emitujący intensywne światło pulsujące do wygładzania skóry, usuwania tatuaży lub włosów lub innych zabiegów na skórze.
6. Sprzęt przeznaczony do stymulacji mózgu za pomocą prądów elektrycznych lub pól magnetycznych lub elektromagnetycznych, które przenikają przez czaszkę, aby zmienić czynność neuronów w mózgu.
Natomiast do wyposażenia wyrobu medycznego zalicza się artykuły, które choć same w sobie nie są wyrobem medycznym, zostały przewidziane przez ich producenta do stosowania łącznie z co najmniej jednym określonym wyrobem medycznym specjalnie po to, by umożliwić używanie tego wyrobu medycznego zgodnie z jego przewidzianym zastosowaniem lub aby konkretnie i bezpośrednio wspomagać medyczną funkcjonalność tego wyrobu medycznego na potrzeby jego przewidzianego zastosowania.
Te kategorie są bardzo szerokie… Jak sprawdzić, do której grupy zalicza się np. nasz sprzęt i w związku z tym, którą treść ostrzeżenia powinniśmy wybrać?
Musimy sprawdzić instrukcję użytkowania i etykietę. Jeżeli będziemy mieli np. sprzęt do usuwania tkanki tłuszczowej lub inny rodzaj produktu z listy powyżej, ale producent nie oznaczy tego sprzętu jako wyrób medyczny, wskaże, że sprzęt ten ma zastosowanie wyłącznie kosmetyczne to będziemy mieli do czynienia z produktem niemającym przewidzianego zastosowania medycznego.
Dlaczego przepis rozporządzenia wymaga, aby w reklamie sprzętu, który nie jest wyrobem medycznym umieszczać ostrzeżenie?
Dzieje się tak, dlatego, że mimo, że nie są one wyrobami medycznymi stosuje się do niech przepisy rozporządzenia MDR, w tym przepisy dotyczące reklamy. Do celów wskazanego rozporządzenia zarówno wyroby medyczne, wyposażenie wyrobów medycznych i produkty wymienione w załączniku XVI do rozporządzenia zwane są łącznie “wyrobami”. Jeżeli zatem dane postanowienie określa wymogi odnośnie „wyrobów” to wymagania te dotyczą również wyposażenia wyrobów medycznych i produktów wymienionych w załączniku XVI do Rozporządzenia MDR.
Czyli wszystkie wymagania dotyczące reklamy obowiązują także dla sprzętów, które nie są wyrobami medycznymi, a zaliczają się do którejś z wymienionych w tym rozporządzeniu kategorii?
Co do zasady tak, zgadza się.
Czy takich urządzeń jest dużo, bo to w sumie nowy wątek. Zastanawiam się, jak dużej grupy osób wykonujących zabiegi może to dotyczyć?
Nie wiem jak dużo, nie posiadam wiedzy w tym zakresie. Jak sądzę zdecydowana większość laserów czy sprzętów emitujących promieniowanie elektromagnetyczne o wysokim natężeniu lub innych sprzętów z listy jest kwalifikowana przez producentów jako wyroby medyczne przeznaczone do używania odpowiednio przez laików lub profesjonalistów.
Zanim przejdziemy dalej, jeszcze podsumujmy. Różnica polega tutaj wyłącznie na treści ostrzeżenia? Cała reszta wymagań dla obu grup jest chyba taka sama, prawda?
Tak, to prawda.
Fragment rozporządzenia:
3. Treść ostrzeżenia, o którym mowa w ust. 1 pkt 3 i ust. 2 pkt 3:
1) w przypadku reklamy w formie audiowizualnej:
a) jest umieszczana w dolnej części reklamy, na płaszczyźnie stanowiącej nie mniej niż 15% jej powierzchni,
b) jest umieszczana w taki sposób, aby tekst wyróżniał się od tła płaszczyzny, był widoczny, czytelny, nieruchomy, umieszczony poziomo, przy czym odległość liter od dolnej i górnej krawędzi tła płaszczyzny reklamy nie może być większa niż 1/2 wysokości liter, a odległość między wierszami napisu nie może być większa niż wysokość liter,
c) jest odczytywana w sposób wyraźny w języku polskim, a czas trwania tego ostrzeżenia nie może być krótszy niż 4 sekundy;2) w przypadku reklamy w formie dźwiękowej jest odczytywana w sposób wyraźny w języku polskim, a czas trwania tego ostrzeżenia nie może być krótszy niż 4 sekundy;
3) w przypadku reklamy w formie wizualnej jest umieszczana:
a) w dolnej części reklamy, na płaszczyźnie stanowiącej nie mniej niż 10% jej powierzchni,
b) w taki sposób, aby tekst wyróżniał się od tła płaszczyzny, był widoczny, czytelny, nieruchomy, umieszczony poziomo, przy czym odległość liter od dolnej i górnej krawędzi tła płaszczyzny reklamy nie może być większa niż 1/2 wysokości liter, a odległość między wierszami napisu jest nie większa niż wysokość liter;4) w przypadku reklamy kierowanej do publicznej wiadomości w formie wizualnej obejmującej więcej niż jedną stronę, umieszcza się na pierwszej stronie.
Dla większości gabinetów najistotniejszy będzie chyba punkt 3 odnoszący się do reklamy wizualnej, czyli grafik reklamowych. Chodzi tutaj o sposób umieszczenia na grafice reklamowej omawianej wcześniej informacji: „To jest wyrób medyczny. Używaj go zgodnie z instrukcją używania lub etykietą.”? Dobrze rozumiem?
Będzie on najistotniejszy dla wszystkich tych gabinetów, które w działalności reklamowej wykorzystują broszury, plakaty, banery, ulotki, katalogi, magazyny i zdjęcia, a więc dla tych gabinetów, które prowadzą działalność reklamą z wykorzystaniem obrazu.
W każdej reklamie w formie wizualnej ostrzeżenie to będzie musiało zostać umieszczone:
1) w dolnej części reklamy, na płaszczyźnie stanowiącej nie mniej niż 10% jej powierzchni,
2) w taki sposób, aby tekst wyróżniał się od tła płaszczyzny, był widoczny, czytelny, nieruchomy, umieszczony poziomo, przy czym odległość liter od dolnej i górnej krawędzi tła płaszczyzny reklamy nie może być większa niż 1/2 wysokości liter, a odległość między wierszami napisu jest nie większa niż wysokość liter;
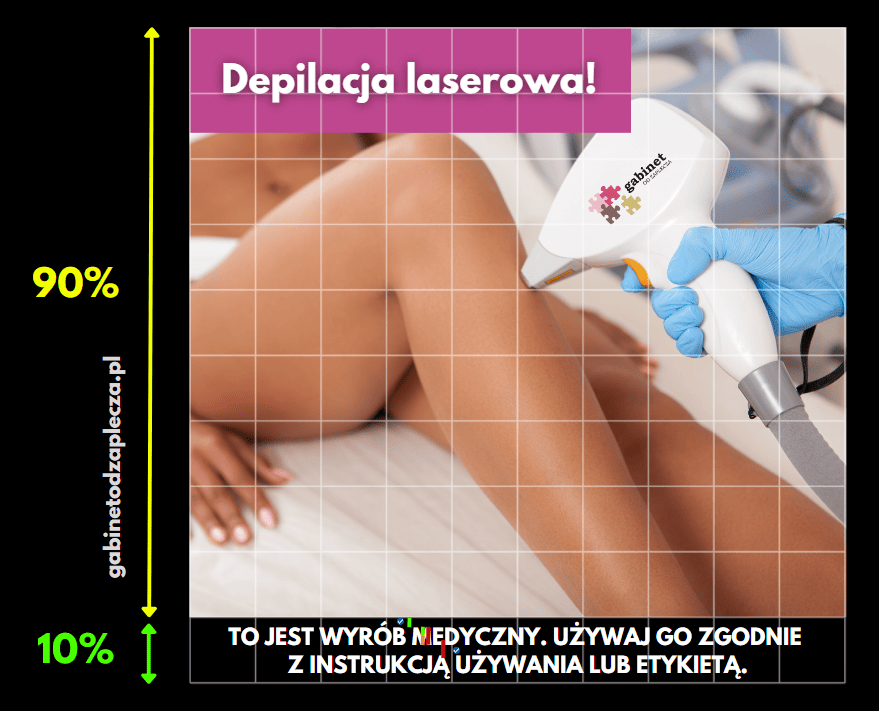
Czyli powinno to wyglądać mniej więcej tak jak na zrobionej przeze mnie grafice?
Zbliżenie na wielkość i odległości liter:


Jeżeli chodzi o samo ostrzeżenie, to zgadza się. Jest na dole, na płaszczyźnie stanowiącej nie mniej niż 10% powierzchni reklamy. Jego tekst wyraźnie odróżnia się od tła, na którym jest, jest widoczny, czytelny, nieruchomy, umieszczony poziomo. Odległość liter od dolnej i górnej krawędzi tła płaszczyzny reklamy nie może jest większa niż 1/2 wysokości liter (zielony pasek), a odległość między wierszami napisu jest nie większa niż wysokość liter (czerwony pasek).
Fragment rozporządzenia:
1. W przypadku, o którym mowa w art. 58 ust. 1 pkt 3 ustawy z dnia 7 kwietnia 2022 r. o wyrobach medycznych, w reklamie wyrobu wskazuje się, że dany przekaz ma charakter reklamowy. Przepis § 3 stosuje się.
2. W przypadkach, o których mowa w art. 58 ust. 1 pkt 5 i 6 ustawy z dnia 7 kwietnia 2022 r. o wyrobach medycznych, w reklamie wyrobu wskazuje się, że dany przekaz ma charakter reklamowy, jeżeli ta informacja nie wynika bezpośrednio i jednoznacznie z tego przekazu.
Jak rozumieć ten fragment?
W ten sposób, że jeżeli będziemy publikować opinie osób, którym zapłaciliśmy (lub wynagrodziliśmy w inny sposób) za złożenie opinii, będziemy musieli:
1) zaznaczyć, że opinia ta ma charakter reklamowy,
2) określić podmiot prowadzący reklamę,
3) wskazać nazwę producenta opiniowanego wyrobu i upoważnionego przedstawiciela, jeżeli został wyznaczony,
4) umieścić ostrzeżenie: „To jest wyrób medyczny. Używaj go zgodnie z instrukcją używania lub etykietą.”
Natomiast w przypadku sponsorowania targów, wystaw, pokazów, prezentacji, konferencji, zjazdów i kongresów naukowych, w tym dla osób wykonujących zawód medyczny lub prowadzących obrót wyrobami lub prezentowania wyrobów w czasie tych wydarzeń należy wskazać, że nasze działania mają charakter reklamowy, jeżeli ta informacja nie wynika bezpośrednio i jednoznacznie z tego przekazu.
Fragment rozporządzenia:
§ 6. Reklama wyrobów, której rozpowszechnianie rozpoczęto przed dniem wejścia w życie rozporządzenia, niespełniająca wymogów w nim określonych, może być rozpowszechniana nie dłużej niż do dnia 30 czerwca 2023 r
Tutaj mamy analogiczny zapis jak w samej ustawie, prawda?
To prawda, ustawa również przewiduje tzw. okres przejściowy do dnia 30 czerwca 2023 r.
Rozporządzenie weszło w życie dnia 13 maja 2023 r., co oznacza, że od tego dnia nowo rozpowszechniane reklamy muszą spełniać wszystkie wymogi tego rozporządzenia.
Reklamy opublikowane przed 13 maja 2023 r., które nie spełniają wymogów Rozporządzenia, będą mogły być rozpowszechniane wyłącznie do dnia 30 czerwca 2023 r.
Oznacza to, że najpóźniej do dnia 30 czerwca 2023 r. musimy dostosować reklamy, które zostały opublikowane przed dniem 13 maja 2023 r. do wymogów określonych w Rozporządzeniu i ustawie o wyrobach medycznych.
Wszystkie reklamy niespełniające tych wymogów nie będą mogły być rozpowszechniane po dniu 30 czerwca 2023 r.
Rozporządzenie wprowadza sporo istotnych zmian i nakłada zupełnie nowe wymogi, przed nami więc kolejna „mała rewolucja”. Mam jednak wrażenie, że nawet ta „stara rewolucja” jeszcze nie do końca zaistniała. Cały czas można znaleźć dużo „starych” reklam wyrobów medycznych, co stwarza wrażenie, że w sumie nic się nie zmieniło. Czy to właśnie przez tę „magiczną” datę 30 czerwca? Na zasadzie, że ok teraz przymykamy oko, bo nikt nie będzie wnikał, która reklama zaczęła być rozpowszechniana wcześniej, a która później, ale po 30 czerwca „zakładamy okulary”.
Myślę, że tak. Trzeba liczyć się z tym, że po upływie okresu przejściowego, czyli właśnie po dacie 30 czerwca 2023 r. reklamy wyrobów medycznych oraz zabiegów wykonywanych przy ich użyciu zaczną być kontrolowane pod kątem ich zgodności z nowymi wymogami.
Sama ustawa obowiązuje już ponad pół roku. Możemy spróbować jakoś podsumować ten okres? Czy pojawiły się jakieś nowe informacje, interpretacje, decyzje? Mam na myśli zarówno same urzędy, jak i środowisko prawnicze. Pytam, bo widziałam też różne spojrzenia na niektóre tematy w Twoim, prawniczym środowisku.
Zgadza się, w środowisku prawniczym pojawiły się poglądy, że kosmetolog nie jest laikiem w rozumieniu ustawy o wyrobach medycznych. To jak wiemy, wciąż pochodna braku porządnej regulacji tego zawodu. Dlatego nie dziwię się, jeżeli ktoś ma odmienne zdanie. To normalne wśród prawników. Żadne stanowisko jakiegokolwiek organu nie tworzy też prawa, a jakikolwiek urząd wyraża tylko swój pogląd.
Dlatego, kto ma rację, dowiemy się dopiero, kiedy dojdzie do nałożenia kary albo jakiegoś sporu, gdzie to sąd będzie musiał rozstrzygnąć tą kwestię. O ile oczywiście wcześniej nie zmieni się prawo.
Ja jednak podtrzymuję swoją opinię, że właśnie z uwagi na braki uregulowania zawodu kosmetologa, kosmetolog nie może być uznany za osobę posiadającą formalne – bo tak to zostało ujęte – wykształcenie w odpowiedniej dziedzinie ochrony zdrowia lub medycyny. A więc w świetle ustawy o wyrobach medycznych jest laikiem. Stanowisko to szerzej wyjaśniam w e-booku.
Na co jeszcze powinniśmy zwrócić uwagę, tworząc reklamy wyrobów medycznych?
Przede wszystkim powinniśmy pamiętać, że Rozporządzenie stanowi jedynie doprecyzowanie niezbędnych danych, jakie ma zawierać reklama, innych niż te określone w ustawie o wyrobach medycznych.
Tworząc reklamę, koniecznie powinniśmy zweryfikować czy jest ona zgodna z wymogami i zasadami określonymi w ustawie o wyrobach medycznych. Powinniśmy też koniecznie zapoznać się z obowiązkami, jakie leżą na osobie uprawnionej do prowadzenia reklamy np. w zakresie przechowywania reklam. Polecam zapoznać się z naszym e-bookiem, gdzie te kwestie są szeroko omówione.
Dziękuję za rozmowę i również zachęcam do lektury naszych materiałów, które są dostępne tutaj.
Na koniec mam dla Ciebie niespodziankę! Żeby uporządkować te wszystkie stare i nowe regulacje, stworzyliśmy bardzo praktyczną listę kontrolną. Jak to działa? Piszesz post, robisz grafikę, nagrywasz film – bierzesz listę kontrolną i punkt po punkcie sprawdzasz, czy Twoja reklama spełnia wszystkie wymogi prawne. Spełnia? Zaznaczasz “ptaszek” i sprawdzasz kolejny punkt. Po odhaczeniu wszystkich “ptaszków” oddychasz z ulgą i publikujesz! 🙂
To proste rozwiązanie uwalnia Cię od konieczności wertowania przepisów i objaśnień, za każdym razem, kiedy chcesz zareklamować zabieg, wstawić post, relację czy rolkę. Możesz się w pełni skoncentrować na tym, co najważniejsze, czyli na promocji swojego biznesu! Po szczegóły wskakuj TUTAJ.
Więcej informacji na temat nowej listy kontrolnej Reklama zabiegu z wyrobem medycznym – co w niej umieścić? znajdziesz TUTAJ. Premierowa zniżka obowiązuje tylko do piątku 23.06!